6 ديسمبر 2016
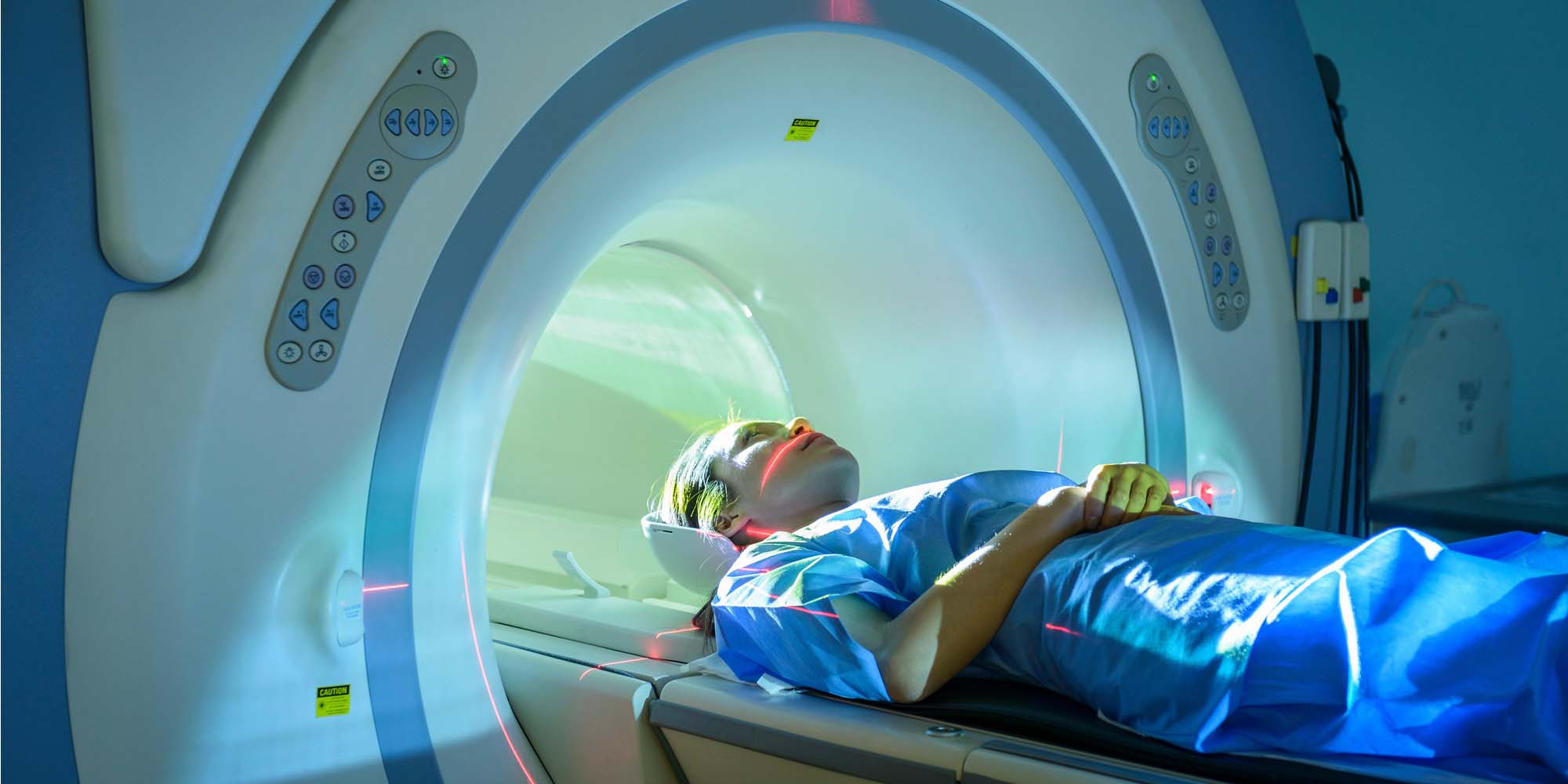
يمكّن التصوير بالرنين المغناطيسيّ الأطبّاء من معاينة ما بداخل الجسم بدرجة كبيرة من التفصيل دون اللجوء إلى الجراحة التوسّعيّة. وبإمكان بعض عوامل التباين زيادة قدرة هذه الأداة التشخيصية لتشمل تشخيص السرطان عن طريق التفاعل مع التغيّرات المرتبطة بالآفات والأورام من قبيل زيادة الحموضة، فالأورام السرطانية ترفع درجة حموضة الوسط المحيط بها.
يُستخدم الأس الهيدروجيني PH للتعبير عن درجة حموضة محلول ما أو قلويّته، ويتراوح من صفر إلى 14. الأرقام التي تفوق سبع درجات تدلّ على قلوية المحلول، في حين تدل الأرقام التي تقلّ عن سبع درجات على أنّ المحلول حمضيّ.
طوّر كازونوري كاتاوكا -من جامعة طوكيو في اليابان- وفريقه البحثي مؤخّرًا1، عامل تبايُن يقوي إشارات الرنين المغناطيسيّ عندما تنخفض درجة الحموضة المحيطة عن 6.7 درجات. وبإمكانه في حال حقن المرضى به إضاءة الأورام وتحسين تبايُن سماتها المرضيّة في فحوصات التصوير بالرنين المغناطيسيّ.
حضّر الباحثون جسيمات نانويّة حسّاسة لدرجة الحموضة -وهي المكوّن الأساسيّ في عامل التباين المطوَّر حديثًا- بواسطة تغليف أيونات المنجنيز وفتات فوسفات الكالسيوم في أغلفة من جليكول بولي إيثيلين. أيونات المنجنيز مصمّمة لتضخيم التصوير بالرنين المغناطيسيّ، في حين أنّ فتات فوسفات الكالسيوم مصمَّم لربط أيونات المنجنيز في ظلّ ظروف عاديّة، ومن ثَمّ إطلاقها عند انخفاض درجة الحموضة إلى قيمة حرجة.
درس كاتاوكا وفريقه كيف تتصرّف هذه الجسيمات النانويّة في مدى مختلف من درجات الحموضة، وشملت درجات الحموضة: 5 وحتى 6 (الحالة داخل الخليّة)، 6.5 وحتى 6.8 (بيئة الورم المصغّرة) ودرجة حموضة (الدم) 7.4. وبعد أربع ساعات، وجدوا أنّ 95%، و71% و36% من أيونات المنجنيز تحررت عن الجسيمات النانوية عند درجات حموضة 5.0، و6.5 و6.7 على التوالي. وبالمقارنة فإنّ أقلّ من 8% من أيونات المنجنيز تحررت عند درجة حموضة بلغت 7.4.
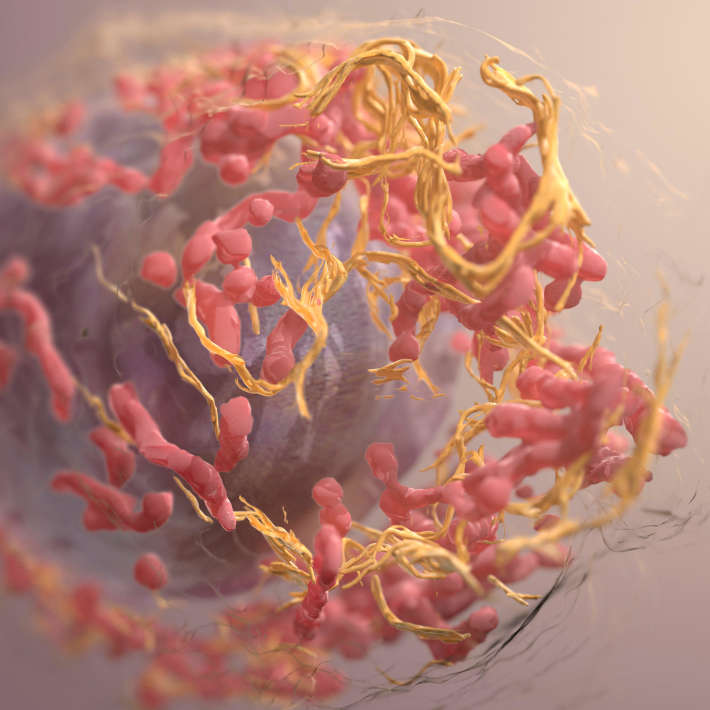
اختبر الباحثون فيما بعد القدرة على التبايُن للجسيمات النانوية في الفئران الحاملة للورم. وتوصّلوا إلى أنّ نسبة الورم/ الأنسجة الطبيعية للجسيمات النانويّة بلغت 130% في غضون 30 دقيقة بعد حقنها عن طريق الوريد. واستمرت النسبة مرتفعة عدّة ساعات، موفّرة الوقت الكافي لإجراء فحوصات التصوير بالرنين المغناطيسيّ. إجمالًا أظهرت النتائج أنّ الجسيمات النانويّة ترتبط بالأورام الصلبة بشكل سريع وانتقائيّ، وتضيئها من خلال إذكاء التباين.
وفي النهاية تحقق كاتاوكا وفريقه مما إذا كان بإمكان جسيماتهم النانويّة تتبُّع أثر الأورام الآخذة في الانتشار. وطبّقوا الجسيمات النانويّة على كبد فأر تخترقه خلايا سرطان القولون، فأضاءت الأورام المنتشرة وكشفت عن مسالك هجرتها في غضون ساعة من الحقن بالجسيمات النانويّة عبر الوريد. وأفاد فريق البحث أنّ تلك الجسيمات كانت صالحة لتشخيص السرطان ولإبراز هجرة الخلايا السرطانيّة للعيان على حدّ السواء.
References
- Mi, P., Kokuryo, D., Cabral, H., Wu, H., Terada, Y. et al. A pH-activatable nanoparticle with signal amplification capabilities for non-invasive imaging of tumour malignancy. Nature Nanotechnology | article