18 أغسطس 2016
يُعَد الضمور نتيجةً مشتركة لكل من فشل القلب الاحتقاني والسرطان، عندما تمر العضلات الهيكلية في الجسم بعملية اضمحلال مستمر. والآن، حدد باحثون آلية خلوية مرتبطة بهذا التدهور، ربما توفر هدفًا مفيدًا للأدوية؛ من أجل الوقاية من هزال العضلات.
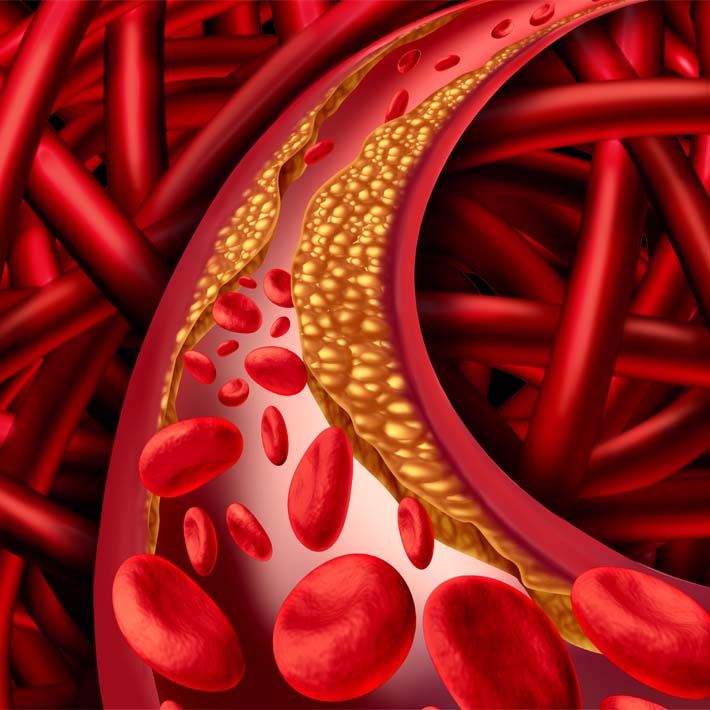
لقد حدد علماء بقيادة جينس فيليتز -من مستشفى شاريتيه الجامعي في برلين، ألمانيا- هرمون أنجيوتنسين الثاني بوصفه محفزًا مميزًا لضمور العضلات لدى مرضى فشل القلب الاحتقاني. ففي أعقاب تضرُّر القلب، تطلَق كميات كبيرة من هذا الهرمون في مجرى الدم. وبدورانه مع الدم، يستثير الهرمون أحداثًا جزيئية تؤدي إلى تدمير انتقائي لبروتينات العضلات. ويمثل بروتين في العضلات -يُدعى RING-finger-1 (MuRF1)- حلقة حيوية في هذه السلسلة، بوصفه الإنزيم الذي يحدد بشكل مباشر البروتينات المقرر التخلُّص منها.
وفي محاولة لتحديد الخطوات الوسيطة في هذه العملية، أجرى فيليتز وزملاؤه بحثًا عن البروتينات التي يمكنها تفعيل الجين الذي يرمّز MuRF1. قادهم مسعاهم إلى بروتين يُعرف بعامل النسخ(TFEB) EB ، يجري إنتاجه بمستويات عالية في كلٍّ من العضلات الهيكلية والقلب، ويرتبط بتسلسلات الحمض النووي في الجينوم المسؤولة عن تنظيم إنتاج MuRF1. ومما يثير الاهتمام، كشْف أبحاث سابقة عن ارتباط TFEB أيضًا بالتحكم في مسارات أخرى معروفة للتحلل البروتيني، على الرغم من أن هذه الدراسة تمثل أول صلة مباشرة بين هذا الجزيء وضمور العضلات.
وواصلت التجارب اللاحقة تعزيز هذه العلاقة. ففي ظل الظروف الطبيعية، تنطوي خلايا العضلات على عمليات مثبطة تمنع TFEB من تحفيز إنتاج MuRF1. ومع ذلك، عند وجود أنجيوتنسين الثاني في مجرى الدم، فإنه يحفز أحداثًا خلوية محددة، تخفف بدورها من هذا التثبيط. ونتيجة لذلك، ترتفع مستويات MuRF1 وتبدأ عملية الضمور. ومن ثَمَّ بيّن الباحثون أن بالإمكان إحباط الضمور الحادث بوساطة أنجيوتنسين الثاني في خلايا العضلات المستزرَعة عن طريق الحد بشكل مباشر من مستويات TFEB أو إزالة الجزيئات التي تخفف من تثبيط TFEB بشكل انتقائي.
يشير مؤلفو الدراسة إلى أن ضمورَ العضلات نتاجُ العديد من العمليات الفسيولوجية المعقدة، بما في ذلك قلة ممارسة مرضى قصور القلب الاحتقاني للنشاط البدني فترة طويلة. لكن ذلك لا ينفي الدور المركزي الراسخ لأنجيوتينسين الثاني، ويعتقد المؤلفون بوجود أدلة قوية في تجاربهم على أن "TFEB أدى دورًا رئيسًا في تنظيم ضمور العضلات الهيكلية الناجم عن أنجيوتنسين الثاني".
ولو مضينا قدمًا في التحقق من صحة هذه النتائج في النماذج الحيوانية، فقد تقدّم العمليات التنظيمية التي تتحكم في نشاط TFEB -في نهاية المطاف- هدفًا وجيهًا لأدوية تهدف إلى إبطاء مسار عملية هزال العضلات أو عكسها.
References
Cheng, W., Pullin, D. I., & Samtaney, R. Angiotensin II Induces Skeletal Muscle Atrophy by Activating TFEB-Mediated MuRF1 Expression. Circ. Res. (2015).| article